En diciembre de 2016 la Autoridad de Fertilización Humana y Embriología (Human Fertilization and Embryology Authority, HFEA) de Gran Bretaña aprobó que las clínicas especializadas de fecundación in vitro de ese país puedan solicitar permiso a dicho organismo para ofrecer a sus clientes la donación mitocondrial en ciertos casos específicos (1).
La decisión se produjo luego de que un panel de científicos independientes convocado por la HFEA publicara su cuarta revisión sobre la seguridad y eficacia de la donación mitocondrial. El panel acordó que la técnica puede ser usada con precaución en ciertos casos en los que los tratamientos alternativos serían de poco o ningún beneficio.
El proceso de transferencia mitocondrial
Todas las mitocondrias del individuo humano se heredan de la madre. Así, si ella es portadora de una mutación en su ADN mitocondrial, sus hijos tendrán la misma mutación.
La donación de las mitocondrias se realiza con la donación del citoplasma donde ellas se encuentran. Esto comporta una técnica muy delicada de transferencia que tiene sus riesgos. El nuevo ser humano resultante tendrá el ADN de su padre y de su madre, más una pequeña cantidad de código genético de una donante.
Las técnicas autorizadas por la HFEA son la Transferencia del huso o núcleo materno (Maternal Spindle Transfer, MST) y la transferencia pronuclear (Pro-Nuclear Transfer, PNT).
Transferencia del huso (núcleo) materno
La transferencia del huso (núcleo) materno (MST) usa un óvulo de la madre con la enfermedad mitocondrial y un óvulo donado de una mujer con mitocondrias sanas. El núcleo del óvulo donado se reemplaza por el núcleo del óvulo de la madre. Esto crearía un óvulo “híbrido“, con el ADN nuclear de la madre y los elementos citoplasmáticos (incluyendo mitocondrias sanas) del donante. Este óvulo híbrido se fertiliza luego por el esperma del padre para crear un embrión humano de tres padres.
Fig. 1: Transferencia del huso (núcleo) materno (MST)
Transferencia pro-nuclear
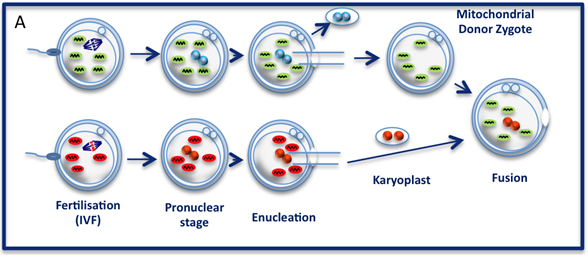
En la transferencia pro-nuclear (PNT) se crea un embrión de una sola célula con el esperma del padre y el óvulo de la madre, cuyas mitocondrias son anormales. Al mismo tiempo, se crea un segundo embrión fertilizando el óvulo de una donante de mitocondrias sanas. Estos embriones de una sola célula (llamados cigotos) son seres humanos en la etapa más temprana de su vida natural. Los “pro-núcleos” (núcleos derivados dela unión espermatozoide-óvulo) son removidos de ambos embriones, destruyéndolos, en un proceso de enucleación. A continuación, se transfiere el pronúcleo del embrión enfermo al citoplasma sano del embrión receptor, resultando así un nuevo embrión.
Esta es una forma de clonación humana destructiva, es decir, el ADN nuclear de un ser humano se utiliza para crear una copia genética o “clon” de ese individuo por transferencia al citoplasma del óvulo de un donante, eliminando el embrión original y el embrión donante en el proceso.
Fig. 2: Transferencia pro-nuclear (PNT)
Regulaciones aprobadas
El Parlamento aprobó regulaciones que permiten los procedimientos de MST y PNT en febrero de 2015, y el marco regulatorio ha estado en vigor desde octubre de 2015, pero los clínicos habían aconsejado esperar hasta después de que la HFEA haya considerado las recomendaciones del panel antes de solicitar permiso para ofrecer el tratamiento a los pacientes. Por lo tanto la decisión de la Autoridad representa otro paso hacia el uso potencial de las técnicas de tratamiento.
Ahora, las clínicas pueden solicitar permiso a la HFEA para ofrecer la donación mitocondrial a los pacientes. El Comité de Licencias de la HFEA evaluará primero la idoneidad de una clínica, mirando a la experiencia del personal existente, habilidad y experiencia, así como su equipo y el entorno en general. Una vez que esta etapa se pase, las clínicas con licencia pueden solicitar permiso al Comité de Aprobación Orgánica para tratar a los pacientes individuales. Sólo cuando estos dos comités han aprobado la solicitud puede comenzar la etapa final, el tratamiento (1).
La primera aplicación aprobada por la HFEA para ofrecer las técnicas es la de Newcastle Fertility at Life. Los pacientes podrán ahora hacer un pedido individualmente a la HFEA para someterse a un tratamiento de donación mitocondrial allí, aunque todavía no se ha aprobado ninguna solicitud (2).
Declaraciones de la presidente de la HFEA
Sally Cheshire, presidente de la HFEA, dijo que “la decisión histórica de hoy significa que los padres con muy alto riesgo de tener un hijo con una enfermedad mitocondrial con amenaza de vida, pronto podrían tener la oportunidad de un niño sano. Esto es cambiar la vida de esas familias”.
Además, se refirió al trabajo del panel de expertos “que revisó el desarrollo, la seguridad y la eficacia de estas técnicas durante cinco años y cuatro informes”, expresando también que la aprobación del Parlamento y puesta a prueba de la opinión pública manifiesta “un enfoque responsable y sostenible de la introducción de nuevos tratamientos de vanguardia en la clínica; […] manteniendo la confianza en el público a medida que avanzamos” (1).
El objetivo centrado en cumplir la expectativa de tener un niño sano puede hacer perder de vista las implicaciones que tiene la técnica. Su uso no se justifica como amortización del tiempo y los valiosos recursos invertidos. Tampoco la confianza y el acompañamiento que puede tener desde la opinión pública, ya que el gran número de la población desconoce el procedimiento en sus detalles específicos y todas las variables en juego, que son nada menos que otras vidas humanas.
Riesgos y objeciones éticas
Como se ha explicado en otro boletín (3), tanto en el procedimiento de transferencia pro-nuclear (PNT), como en el de transferencia del núcleo materno (MST), hay riesgo de dañar el núcleo transferido o el embrión/citoplasma anfitrión, causando que el desarrollo del embrión resultante sea anormal.
Estos procedimientos son formas de “ingeniería de línea germinal” que alteran la composición genética de las generaciones futuras de una manera permanente.
La heteroplasmia mitocondrial, es decir la persistencia de algunas mitocondrias de la madre en el óvulo del donante a causa del arrastre en la transferencia, es un riesgo significativo (4) para cualquier niño producido por estas técnicas.
Se introduce una disparidad permanente e innatural entre el genoma nuclear y el genoma mitocondrial que será heredado por todas las generaciones posteriores. En algunas especies (5), la incompatibilidad entre la mitocondria y el genoma nuclear compromete significativamente la salud del individuo.
En el caso de la MST, sin perjuicio de las objeciones éticas inherentes a las técnicas de procreación artificial, los problemas no refieren al derecho a la vida, ya que para generar el óvulo híbrido madre-donante, se destruyen dos óvulos sin fecundar, manipulando sólo células humanas. Dado que la vida humana comienza (6) en el momento de la fusión esperma-óvulo, en la PNT, en cambio, estamos ante una clonación eugenésica en la que se eliminan seres humanos (embriones), utilizando luego sus partes para crear un nuevo ser humano con un estado biológico mejorado.
La opinión de que la transferencia del núcleo de un cigoto no es más que un enfoque “terapéutico” para el tratamiento de la enfermedad, sería cierta si un ser humano fuera nada más que su ADN. El embrión producido por este procedimiento no es sólo el niño original de los padres, movido a un nuevo “medio ambiente” citoplasmático. Mientras que nuestro ADN nuclear único determina claramente muchos aspectos de nuestras características individuales, también estamos muy influenciados por la composición específica no genética del óvulo que nos produce (3).
Muchos aspectos del desarrollo embrionario y por lo tanto del individuo único que acabamos siendo, dependen de componentes no genéticos derivados del citoplasma del óvulo (6).
La importancia de los factores no genéticos en la determinación del carácter singular de un individuo humano está muy claramente ilustrada por las “mutaciones de efecto materno“(7). Estas mutaciones no tienen ningún efecto en el desarrollo o la función de la madre, pero específicamente perturban el desarrollo de los embriones derivados de sus óvulos.
Como la opinión pública desconoce, en general, estas particularidades de la donación mitocondrial, la labor informativa se vuelve así obligatoria para que se vea libre de coacciones a la hora de valorar el impacto real de estas técnicas en la vida de las personas.
Informe de Selva Luz Contardi
Referencias
(1) HFEA permits cautious use of mitochondrial donation in treatment, following advice from scientific experts (Dic 2016) http://www.hfea.gov.uk/10563.html
(2) HFEA statement on mitochondrial donation (Mar 2017) http://www.hfea.gov.uk/10635.html
(3) No somos sólo nuestro ADN: Los peligros éticos de los embriones de 3 padres https://centrodebioetica.org/web/2014/04/no-somos-solo-nuestro-adn-los-peligros-eticos-de-los-embriones-de-3-padres/
(4) Yabuuchi, A et al. Prevention of mitochondrial disease inheritance by assisted reproductive technologies: prospects and challenges. (2012). https://www.ncbi.nlm.nih.gov/pubmed/22085724
(5) Meiklejohn, CD et al. An Incompatibility between a mitochondrial tRNA and its nuclear-encoded tRNA synthetase compromises development and fitness in Drosophila. (2013) https://www.ncbi.nlm.nih.gov/pubmed/23382693
(6) Condic, ML. When Does Human Life Begin? A Scientific Perspective (The Westchester Institute for Ethics & the Human Person, 2008). http://marahjoyneice.pbworks.com/w/file/105932706/wi_whitepaper_life_print.pdf
(7) Matzuk, MM. Genetics of mammalian reproduction: modeling the end of the germline. (2012) https://www.ncbi.nlm.nih.gov/pubmed/22335799


